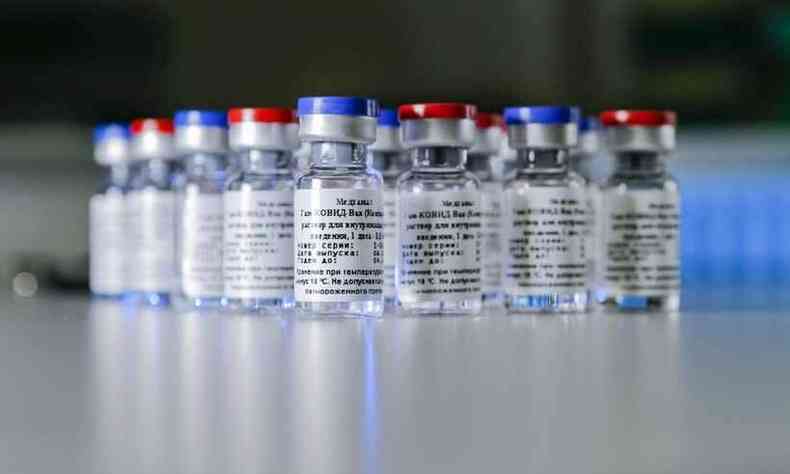
O presidente Vladimir Putin afirmou que a R�ssia se tornou o primeiro pa�s do mundo a provar a regulamenta��o da vacina nesta ter�a-feira, 11. O governo do Paran� deve anunciar na quarta-feira, 12, um acordo com o Minist�rio de Sa�de russo para a produ��o de uma vacina contra o coronav�rus. O acordo prev� que o Estado realize testes, produza e distribua a vacina.
A ag�ncia tamb�m afirmou que n�o pode prever o tempo necess�rio para dar o aval ao uso da droga. "A Anvisa tem a fun��o de avaliar os pedidos de registro e autoriza��es de estudos apresentados pelos laborat�rios farmac�uticos que tem interesse em colocar seus medicamentos e vacinas no Brasil. A avalia��o da Anvisa tem foco na seguran�a e efic�cia que s�o os requisitos fundamentais para qualquer medicamento ou vacina."
Os estudos sobre a vacina russa geram d�vida na comunidade cient�fica. O Minist�rio da Sa�de da R�ssia informa que as pesquisas para a vacina est�o na fase 3, a �ltima e mais importante das etapas de produ��o de uma vacina, mas n�o divulgou estudos em nenhuma revista cient�fica sobre os resultados, dura��o e os detalhes das fases anteriores. Al�m disso, a vacina foi aprovada ap�s menos de dois meses do in�cio dos testes em humanos.
Segundo a Anvisa, o desenvolvimento de medicamentos passa por tr�s principais etapas: 1) desenvolvimento explorat�rio, 2) pesquisa pr�-cl�nica, 3) pesquisa cl�nica (uso em humanos). Ap�s o fim dos estudos, a empresa pede o registro da droga na ag�ncia sanit�ria. O aval � necess�rio para comercializar ou distribuir a droga no Pa�s.
"� no momento do registro que � verificado se a vacina � fabricada e controlada dentro dos padr�es de qualidade esperados pelos regulamentos t�cnicos e que os dados de seguran�a e efic�cia s�o avaliados", disse a ag�ncia.
A Anvisa informou que editou uma s�rie de regras para priorizar an�lises que tratam do novo coronav�rus. "As solicita��es tem sido avaliadas pela Anvisa no prazo de 72 horas. Para conseguir este prazo foram realizadas reuni�es com a empresas e acionado o comit� de avalia��o de estudos cl�nicos, registros e mudan�as p�s-registros de medicamentos para preven��o ou tratamento da Covid-19, que � uma estrutura interna da Anvisa."
