Vacina bivalente est� indicada para imuniza��o contra o coronav�rus e pode ser utilizada por pessoas a partir de 5 anos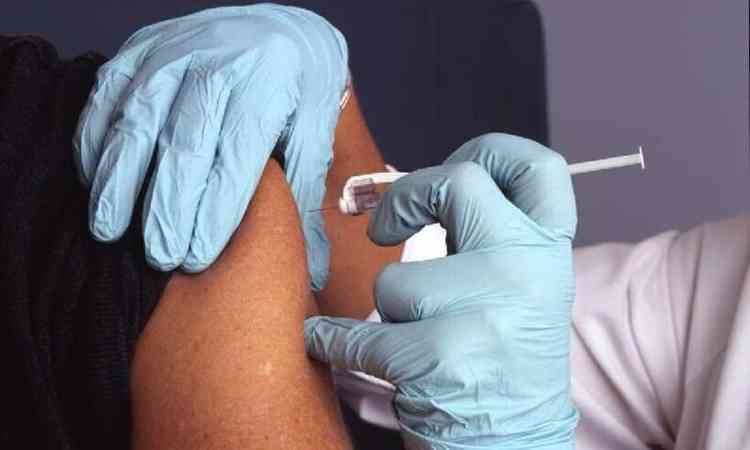
A Ag�ncia Nacional de Vigil�ncia Sanit�ria (Anvisa) aprovou, nesta segunda-feira (24/7), o registro da vacina Comirnaty bivalente contra a covid-19 . O produto � fabricado pelo laborat�rio farmac�utico Pfizer. Esta � a segunda bivalente a ser aprovada pela ag�ncia reguladora.
O que s�o vacinas bivalentes?
Vacinas bivalentes conferem maior prote��o contra a covid-19, pois cont�m uma mistura de cepas do v�rus Sars-CoV-2. A Comirnaty bivalente � constitu�da pela variante original (cepa Wuhan) e uma variante de circula��o mais recente (cepa �micron).
Esta � a segunda vacina bivalente registrada de forma definitiva para uso no Brasil, sendo que ela j� estava sendo utilizada no Programa Nacional de Imuniza��es (PNI) do Minist�rio da Sa�de, ap�s receber aprova��o da Anvisa para uso emergencial.
Entenda o registro da vacina
A Comirnaty bivalente foi aprovada considerando os requisitos exigidos pela Resolu��o da Diretoria Colegiada (RDC) 55/2010, que trata do registro de produtos biol�gicos, inclu�das as vacinas. O registro � o padr�o ouro de avalia��o, com base em dados consolidados.
A vacina j� est� autorizada pela Ag�ncia Europeia de Medicamentos (European Medicines Agency – EMA) e pela ag�ncia reguladora dos Estados Unidos (Food and Drug Administration – FDA), entre outras.



*Para comentar, fa�a seu login ou assine