*O t�tulo e o texto da reportagem foram atualizados na ter�a (12/1).
O governo de S�o Paulo anunciou, nesta ter�a-feira (12/01), os resultados dos testes de efic�cia da CoronaVac , a vacina da farmac�utica chinesa Sinovac que est� sendo desenvolvida no Brasil em parceria com o Instituto Butantan.
De acordo o diretor de pesquisa do Instituto Butantan, Ricardo Pal�cios, os estudos apontaram que a efic�cia geral da vacina � de 50,38%. O dado foi obtivo com testes feitos em 12.508 volunt�rios no pa�s, todos profissionais de sa�de. Segundo Pal�cios, os profissionais de sa�de foram escolhidos porque t�m uma exposi��o maior ao v�rus.
Esse dado � a taxa global de efic�cia da CoronaVac, ou seja, os desfechos prim�rios, que incluem todas as pessoas que ficaram doentes independentemente da gravidade da doen�a.
"[O teste] n�o � a vida real exatamente. � um teste artificial, no qual selecionamos dentro das popula��es poss�veis, selecionamos aquela popula��o que a vacina poderia ser testada com a barra mais alta. A gente quer comparar os diferentes estudos, mas � o mesmo que comparar uma pessoa que faz uma corrida de 1km em um trecho plano e uma pessoa que faz uma corrida de 1 km em um trecho �ngreme e cheio de obst�culos. Fizemos deliberadamente para colocar o teste mais dif�cil para essa vacina, porque se a vacina resistir a esse teste, iria se comportar infinitamente melhor em n�veis comunit�rios", afirmou Ricardo Pal�cios no an�ncio.
O pedido de uso emergencial da vacina foi feito � Anvisa na sexta-feira, segundo o Butantan.
A taxa global de efic�cia recomendada pela Organiza��o Mundial da Sa�de (OMS) e pela Anvisa � de, ao menos, 50%. As duas etapas anteriores da pesquisa feitas no Brasil j� haviam atestado que a CoronaVac � segura e produz uma resposta do sistema imunol�gico, de acordo com o governo de S�o Paulo.
Dimas Covas, diretor do Butantan, disse que a vacina "tem seguran�a, efic�cia e tem todos os requisitos que justificam seu uso emergencial."
Pal�cios explicou que o instituto foi extremamente rigoroso nos estudos. "Na defini��o de casos que utilizamos, usamos os sintomas mais abrangentes poss�vel. Outros estudos n�o incluiriam como caso dois dias de dor de cabe�a, dois dias de coriza. Foi uma defini��o extremamente abrangente para poder capturar at� o caso mais leve poss�vel", afirmou.
O Butantan n�o digvulgou qual seria a cobertura vacinal necess�ria da CoronaVac para impedir o avan�o da covid-19. Embora a vacina seja extremamente segura e tenha efic�cia contra o v�rus, ainda n�o h� dados que mostrem que ela � capaz de erradicar a pandemia, explicou Pal�cios. "Ela vai erradicar, eliminar a doen�a? O estudo n�o permite determinar isso. Precisaremos fazer estudos de efetividade, nos quais a gente verifique qual impacto que tem em geral nas comunidades vacinadas", afirmou.
Confus�o com dados anteriores
Na semana passada o instituto havia divulgado dados preliminares de que a vacina evitou 78% de casos leves e prote��o total (100%) contra mortes, casos graves e interna��es nos volunt�rios vacinados que foram contaminados. Nenhum dos infectados precisou de interna��o hospitalar, informou o Instituto Butantan. A aus�ncia da efic�cia geral no anunciou anterior foi alvo de muitas cr�ticas de cientistas e profissionais de sa�de e gerou uma confus�o, levando algumas pessoas a pensarem que o dado de 78% era o dado de efi�cia geral.
Nesta segunda-feira (11/01), a CoronaVac foi aprovada pelas autoridades sanit�rias da Indon�sia. Os testes cl�nicos de fase 3 feitos neste pa�s do Sudeste Asi�tico indicaram uma taxa de efic�cia global de 65,3%. A previs�o � que as campanhas de imuniza��o sejam iniciadas por l� na quarta-feira (13/01).
A taxa global de efic�cia recomendada pela Organiza��o Mundial da Sa�de (OMS) e pela Anvisa � de, ao menos, 50%. As duas etapas anteriores da pesquisa feitas no Brasil j� haviam atestado que a CoronaVac � segura e produz uma resposta do sistema imunol�gico, de acordo com o governo de S�o Paulo.
- OMS:�vacina obrigat�ria contra covid-19 pode ser necess�ria em�pa�ses com baixa ades�o volunt�ria e alto cont�gio�
- Vacina contra covid-19: pa�ses ricos reservam doses e deixam pa�ses pobres sem, adverte alian�a
A fase 3 da pesquisa investigava se ela de fato impedia que uma pessoa ficasse doente ao ser infectada pelo Sars-Cov-2.
Originalmente, o governo paulista previa divulgar uma an�lise preliminar da efic�cia em 15 de dezembro, mas concluiu que j� tinha condi��es de fazer uma an�lise completa dos resultados, porque j� tinha ao menos 170 volunt�rios com casos de covid-19 confirmados, um par�metro estabelecido pelo protocolo do estudo, e adiou o an�ncio para janeiro.
Com base nesta s�rie de resultados, o governo paulista e o Butantan enviaram � Anvisa o pedido de autoriza��o para o uso emergencial e o registro definitivo da vacina no pa�s.
De acordo com informa��es divulgadas no s�bado (09/01), a Anvisa rejeitou parte da documenta��o enviada pelo Butantan e requisitou novos dados sobre as pesquisas. Pedidos como este s�o normais e fazem parte do processo de avalia��o antes da aprova��o para uso geral.
Em 21 de dezembro, a ag�ncia j� havia feito a certifica��o da f�brica da CoronaVac na China, ap�s fazer uma inspe��o nas instala��es. Este � um dos pr�-requisitos para o registro da vacina no Brasil.
Obter o aval da ag�ncia ser� fundamental para que o governo de Jo�o Doria (PSDB) consiga colocar em pr�tica o plano de vacina��o no Estado de S�o Paulo, com previs�o de in�cio em 25 de janeiro.
Simultaneamente, a Sinovac dever� pedir o registro da vacina � Administra��o Nacional de Produtos M�dicos, a equivalente da Anvisa na China. A expectativa � que o registro seja concedido em tr�s dias.
Isso dever� pressionar a ag�ncia brasileira, porque a lei 13.979 obriga a Anvisa a conceder autoriza��o "excepcional e tempor�ria" para medicamentos considerados essenciais no combate � pandemia que tenham sido registrados pela ag�ncias do Jap�o, da China, dos Estados Unidos ou da Europa.
A autoriza��o tem que ser concedida at� em 72 horas ap�s o pedido ser feito � ag�ncia brasileira. Caso a Anvisa n�o se manifeste, isso ocorre automaticamente. O prazo normal para an�lise de registro permanente de vacinas contra a covid-19 � de at� 60 dias.
Esse trecho da lei chegou a ser vetado pelo presidente Jair Bolsonaro (sem partido), mas o veto foi derrubado pelo Congresso Nacional.
O entendimento da lei foi ratificado pelo ministro Ricardo Lewandowski, do Supremo Tribunal Federal (STF), que concedeu uma liminar neste sentido em 17 de dezembro. A quest�o ainda ser� apreciada pelo plen�rio da Corte.
Quais s�o as vantagens e desvantagens da tecnologia da CoronaVac?
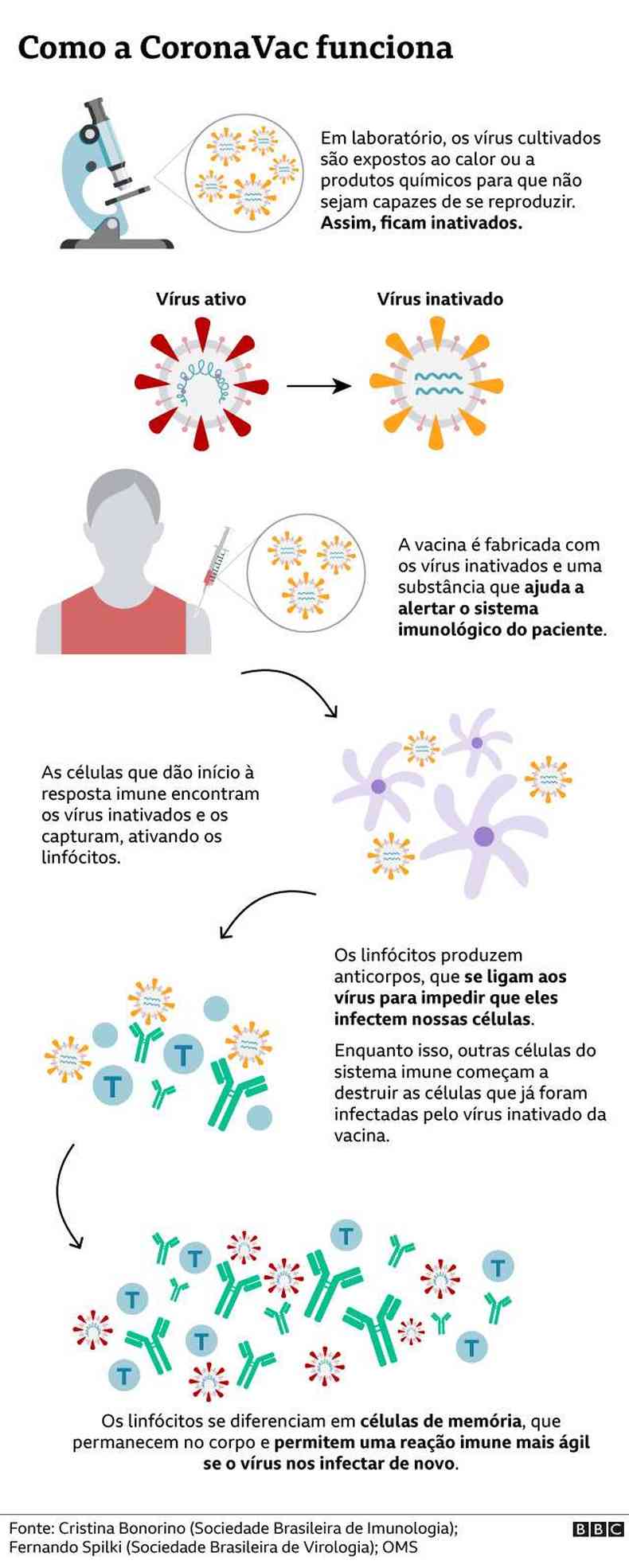
A vacina da Sinovac usa uma tecnologia bastante tradicional de imuniza��o, desenvolvida h� cerca de 70 anos, diz o imunologista Aguinaldo Pinto, professor da Universidade Federal de Santa Catarina.
"N�o h� nada de novo na tecnologia por tr�s dessa vacina. Temos muitas vacinas de v�rus inativados sendo comercializadas hoje", afirma Pinto.
Entre as que tomamos de rotina que utilizam essa tecnologia, est�o as de gripe, hepatite A e poliomielite (na vers�o injet�vel).
A seu favor, conta a experi�ncia de d�cadas no seu uso em sa�de p�blica.
E tamb�m sua seguran�a, porque � um imunizante baseado em v�rus inativados, ou seja, que n�o s�o capazes de se reproduzir. Por isso, eles n�o conseguem deixar uma pessoa doente.
Mesmo assim, a vacina consegue gerar a rea��o imunol�gica desejada e criar no nosso organismo uma mem�ria de como nos defender contra essa amea�a.
No caso da CoronaVac, s�o aplicadas duas doses, com uma diferen�a de 21 dias entre elas.
Mas vacinas com essa tecnologia s�o mais caras para serem produzidas, porque � necess�rio cultivar uma grande quantidade de v�rus em laborat�rio, que devem ent�o ser submetidos ao processo de inativa��o.
Al�m disso, elas n�o precisam ser armazenadas em temperaturas extremamente baixas, como � o caso a vacina da Pfizer e da Moderna, que devem ser mantidas a -70�C e -20�C respectivamente para durarem mais tempo.
A CoronaVac � armazenada e transportada a uma temperatura de refrigeradores comuns, entre 2�C e 8�C, o que facilita a log�stica de um plano de imuniza��o.

Como � feita a produ��o pelo Butantan?
O instituto come�ou a produzir a vacina em 9 de dezembro. "� a primeira vacina contra a covid-19 produzida no Brasil", disse Dimas Covas, diretor do Butantan, ao anunciar a fabrica��o.
O Butantan adotou desde ent�o um regime de trabalho intensivo para ter prontas em janeiro 40 milh�es das 46 milh�es de doses que o governo de S�o Paulo espera ter em m�os em janeiro.
Outras 6 milh�es s�o importadas da China, das quais 4,22 milh�es j� chegaram ao Brasil.
O instituto anunciou que a produ��o est� ocorrendo em turnos sucessivos, sete dias por semana, para que a produ��o di�ria alcance a capacidade de 1 milh�o de doses por dia.
Desta forma, a f�brica funciona sem parar, 24 horas por dia, para dar conta da demanda. At� outubro, a opera��o era de segunda a sexta-feira, em dois turnos.
A for�a de trabalho tamb�m foi ampliada em 50% para dar conta da demanda.
Como ser� a vacina��o em SP
O governo de S�o Paulo anunciou em 7 de dezembro que a vacina��o com a CoronaVac ter� in�cio em 25 de janeiro, embora ela n�o tenha sido aprovada ainda pela Anvisa.
Por enquanto, foram anunciados os detalhes apenas da primeira fase do plano de imuniza��o, que tem como p�blico-alvo profissionais de sa�de, pessoas com mais de 60 anos, ind�genas e quilombolas.
De acordo com o governo paulista, estes grupos respondem por 77% das mortes causadas pelo novo coronav�rus no Estado.
Isso implicar� na vacina��o de 9 milh�es de pessoas e no uso de 18 milh�es de doses.
A vacina��o ser� gratuita e realizada por meio de 10 mil postos de vacina��o, dos quais 4,8 mil ser�o novos locais, criados especialmente para a campanha, com o uso provis�rio de escolas, quart�is e farm�cias, por exemplo.
Na quarta-feira (06/01), o governo de S�o Paulo divulgou que a vacina��o ocorrer� de segunda a sexta, das 7h �s 22h, e de 7h �s 17h aos s�bados, domingos e feriados.
A previs�o � que a primeira fase do plano esteja conclu�da at� 28 de mar�o, quando o governo paulista estima que 20% dos 46 milh�es de habitantes do Estado estar�o imunizados.
A primeira fase do plano seguir� o seguinte calend�rio, para evitar aglomera��es nos postos de sa�de:
* profissionais da Sa�de, ind�genas e quilombolas: 25/01 (1� dose) e 15/02 (2� dose);
* pessoas com 75 anos ou mais: 08/02 (1� dose) e 01/03 (2� dose);
* pessoas com 70 a 74 anos: 15/02 (1� dose) e 03/03 (2� dose);
* pessoas com 65 a 69 anos: 22/02 (1� dose) e 15/03 (2� dose)
* pessoas com 60 a 64 anos: 01/03 (1� dose) e 22/03 (2� dose)
Cada grupo dever� procurar os postos de vacina��o ao longo da semana seguinte ap�s a data de in�cio. O atendimento ser� das 7h �s 22h de segunda a sexta e das 7h �s 17h aos s�bados, domingos e feriados.
Tudo ser� feito apenas pelo sistema p�blico de sa�de, e n�o h� previs�o por enquanto de aplica��o na rede privada.
O governador Jo�o Doria disse que n�o ser� preciso comprovar a resid�ncia no Estado para ser vacinado. "Todo e qualquer brasileiro que estiver em solo do Estado e pedir a vacina ser� vacinado", afirmou.
Ainda n�o foram divulgados detalhes sobre as pr�ximas etapas do plano de imuniza��o.
A CoronaVac vai estar dispon�vel em outros locais do pa�s?
� prov�vel que sim. Mas as condi��es em que isso vai acontecer ainda s�o incertas.
O governo de S�o Paulo disse que disponibilizar� 4 milh�es das 46 milh�es de doses j� compradas para que outros Estados imunizem profissionais de sa�de.
De acordo com Doria, 11 j� manifestaram interesse: Acre, Cear�, Esp�rito Santo, Maranh�o, Mato Grosso do Sul, Par�, Piau�, Para�ba, Rio Grande do Norte, Rio Grande do Sul e Roraima.
Doria tamb�m informou que mais de 900 munic�pios j� manifestaram interesse na vacina, mas a rela��o n�o foi divulgada.
Por sua vez, o ministro da Sa�de, o general Eduardo Pazuello, chegou a anunciar no final de outubro a compra de 46 milh�es doses da CoronaVac.
Mas foi no dia seguinte desautorizado pelo presidente Jair Bolsonaro (sem partido) em uma mensagem pelo Facebook na qual disse que, como o imunizante ainda n�o tinha sido autorizado pela Anvisa, sua decis�o era de "n�o adquirir a referida vacina".
Bolsonaro e Doria s�o advers�rios pol�ticos e provavelmente se enfrentar�o nas urnas em 2022.
Questionado por Doria em uma reuni�o com governadores em 8 de dezembro, Pazuello disse que compraria a CoronaVac, uma vez que ela esteja registrada na Anvisa, "se houver demanda e houver pre�o".
Ao lan�ar o plano oficial no �ltimo dia 16 , o Minist�rio da Sa�de indicou que havia uma inten��o de compra da Coronavac, mas n�o especificou a princ�pio quantas doses pretendia adquirir.
No dia seguinte, Pazuello informou que o plano prev� receber 9 milh�es de doses da CoronaVac em janeiro e 22 milh�es em fevereiro.
Ainda n�o h� uma data prevista para o in�cio da campanha nacional de imuniza��o contra a covid-19.
Vai ser obrigat�rio tomar a vacina?
Jo�o Doria disse em meados de outubro que a vacina contra a covid-19 seria obrigat�ria em todo o Estado de S�o Paulo. Segundo o governador, somente quem tiver um atestado m�dico que comprove que ele n�o pode ser imunizado seria liberado.
"Adotaremos medidas legais se houver contrariedade nesse sentido", disse o governador na �poca.
No mesmo dia, Bolsonaro afirmou que quem ofereceria vacinas contra a covid-19 seria o Minist�rio da Sa�de, mas "sem impor ou tornar a vacina obrigat�ria".
Em meio a esse embate, o Supremo Tribunal Federal (STF) se manifestou sobre o assunto ao julgar duas a��es levadas � corte relativas � lei criada em fevereiro que prev� medidas de combate � pandemia, entre elas a possibilidade de vacina��o obrigat�ria.
Uma era movida pelo PDT, que pede que o STF reconhe�a o direito de Estados e munic�pios de impor a vacina��o. Outra, pelo PTB, defende que essa possibilidade � inconstitucional. Ambas s�o relatadas pelo ministro Ricardo Lewandowski.
O STF decidiu por ampla maioria no �ltimo dia 17 que Uni�o, Estados e munic�pios podem adotar medidas para obrigar a popula��o a se vacinar, mas n�o poder�o for�ar fisicamente as pessoas a fazer isso.
A Corte autorizou no entanto que sejam adotadas san��es indiretas, como proibir os n�o vacinados de frequentar certos lugares ou exercer determinadas atividades.
Eles ressaltaram que a vacina��o generalizada da popula��o � necess�ria para reduzir a circula��o do coronav�rus, salvando vidas. J� s�o mais de 180 mil mortos pela covid-19 no Brasil.
Ao comentar a decis�o, Bolsonaro disse que o governo federal n�o tomar� medidas contra quem n�o quiser se vacinar e que a decis�o do Supremo pode ser "in�cua", porque "n�o vai ter vacina para todo mundo".
Doria n�o se manifestou sobre o assunto desde a decis�o do STF.
J� assistiu aos nossos novos v�deos no YouTube ? Inscreva-se no nosso canal!

/imgsapp.em.com.br/app/autor/2021/05/07/fotos/20210507125942860406i.jpg)