A Ag�ncia Nacional de Vigil�ncia Sanit�ria (Anvisa) autorizou, nesta ter�a-feira (25/05), testes do soro anti-COVID em seres humanos. O produto, desenvolvido pelo Instituto Butantan, ser� usado em pacientes infectados pelo novo coronav�rus.
Os testes em humanos ir�o verificar a seguran�a e a efic�cia do soro contra a COVID-19.
De acordo com o Butantan, h� tr�s mil frascos prontos para serem testados em humanos. A previs�o � de que eles comecem a ser aplicados a partir das pr�ximas semanas. Ser� a primeira vez em que humanos receber�o esse soro.
O material n�o � para a preven��o da doen�a. O objetivo do soro, conforme o Butantan, � atuar no tratamento da enfermidade e evitar que o paciente desenvolva quadro grave.
O primeiro passo para a obten��o do soro foi isolar o novo coronav�rus em materiais coletados de um paciente brasileiro infectado. Depois, esse v�rus foi cultivado em laborat�rio, inativado por radia��o — com apoio do Instituto de Pesquisas Energ�ticas e Nucleares (IPEN) — e submetido a v�rios testes em camundongos, para assegurar que n�o traria riscos.
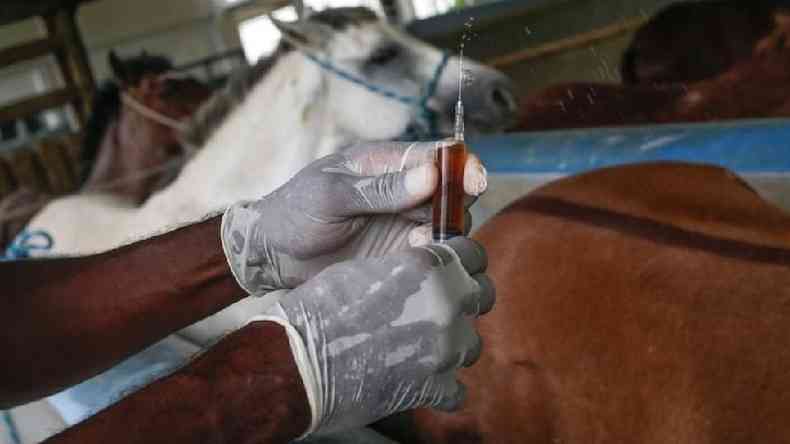
O v�rus inativado foi aplicado em cavalos. Ap�s receberem o material, esses animais produziram anticorpos. Depois, o plasma resultante (a por��o l�quida do sangue que cont�m fatores de coagula��o, anticorpos e outras prote�nas) foi coletado e processado pelo Butantan. A partir de ent�o, surgiu o soro.
Na fase pr�-cl�nica, pesquisadores do Butantan fizeram um "teste de desafio" em parceria com a Universidade de S�o Paulo (USP). Nele, camundongos e coelhos foram infectados pelo novo coronav�rus e receberam o soro. Segundo o Instituto, houve diminui��o da carga viral desses animais, al�m de preserva��o da estrutura pulmonar deles.
Desde mar�o, o Instituto Butantan tenta a aprova��o do soro para testes em humanos. Na �poca, a Anvisa avaliou o pedido e deu anu�ncia para a pesquisa em brasileiros, mas depois pediu mais informa��es, o que fez com que os estudos cl�nicos fossem adiados.
Na semana passada, o diretor do Instituto, Dimas Covas, disse que a demora da Anvisa, vinculada ao Minist�rio da Sa�de, representava inseguran�a da ag�ncia, que, segundo ele, sempre se pronuncia ap�s outras entidades internacionais.
"Quando se submete � Anvisa pela primeira vez um soro, existe uma dificuldade l�, uma inseguran�a. Porque essa decis�o vai valer pro mundo inteiro", declarou, durante reuni�o p�blica virtual na Assembleia Legislativa de S�o Paulo.
A Anvisa avaliou a proposta de pesquisa integralmente, sem apoio de ag�ncias estrangeiras, porque as fases iniciais s�o feitas somente no Brasil. A ag�ncia argumenta que, por se tratar da primeira vez que o material seria testado em pessoas, precisou fazer uma "avalia��o criteriosa dos aspectos t�cnicos e de seguran�a do produto".
Quem receber� o soro?
Os estudos cl�nicos do soro anti-COVID ser�o feitos em parceria com o Hospital do Rim e Hipertens�o e com o Hospital das Cl�nicas da Faculdade de Medicina da USP.
De acordo com nota divulgada pelo Butantan no come�o de mar�o, os primeiros humanos a receberem o soro ser�o pacientes transplantados do Hospital do Rim, com o m�dico nefrologista Jos� Medina, e pacientes com comorbidades no Hospital das Cl�nicas da Universidade de S�o Paulo, com o m�dico infectologista Esper Kallas.
O material ser� utilizado em pacientes com infec��o recente e alto ou alt�ssimo risco de doen�a grave pelo novo coronav�rus.
O objetivo da pesquisa � verificar a seguran�a, apontar a dose mais apropriada e descobrir a efic�cia do soro em pacientes com quadro inicial de sintomas de COVID-19. A expectativa � de que esses pacientes n�o desenvolvam quadro grave da doen�a.
Um dos argumentos para atestar a seguran�a do teste do material em humanos � que o plasma dos cavalos j� � utilizado na fabrica��o de soros, como antirr�bico, pe�onhento (serpentes), artr�pode (aranhas), antitet�nico e botul�nico.
No in�cio de mar�o, Dimas Covas declarou que os estudos em animais apontaram que o soro anti-COVID "� extremamente efetivo". Por isso, disse, a expectativa � de que a mesma efetividade seja demonstrada nos estudos em humanos.
Ap�s os testes em hospitais, os resultados ser�o apresentados � Anvisa. A partir disso, o Butantan poder� pedir a autoriza��o para o uso do soro como tratamento contra a COVID-19.
J� assistiu aos nossos novos v�deos no YouTube ? Inscreva-se no nosso canal!

/imgsapp.em.com.br/app/autor/2021/05/07/fotos/20210507125942860406i.jpg)