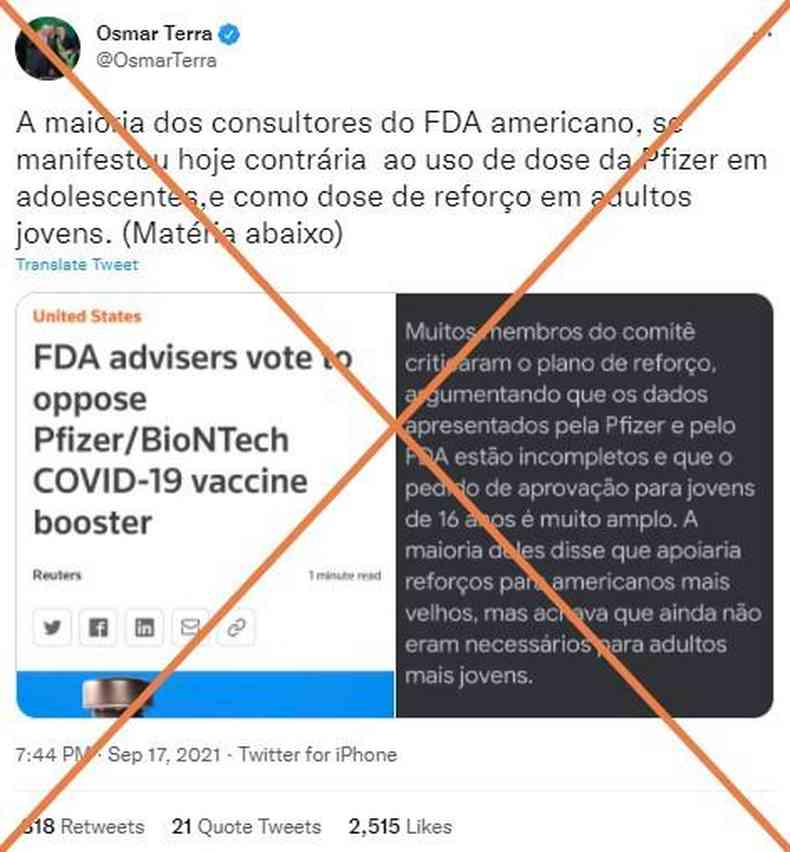
A alega��o foi difundida inicialmente pelo deputado federal Osmar Terra (MDB) no Twitter. “A maioria dos consultores do FDA americano, se manifestaram hoje contr�rios ao uso de dose da Pfizer em adolescentes. E como dose de refor�o em adultos jovens” , escreveu o tamb�m ex-ministro da Cidadania do governo de Jair Bolsonaro.
Logo, capturas de tela do tu�te - ilustrado com mat�rias sobre uma vota��o realizada no �ltimo dia 17 de setembro - come�aram a circular no Facebook ( 1 , 2 , 3 ).
A vota��o mencionada pelo deputado n�o foi, contudo, sobre a vacina��o de adolescentes contra a covid-19 de maneira geral, mas sobre a aplica��o da terceira dose do imunizante da Pfizer-BioNTech para todos com 16 anos ou mais.
Dose de refor�o
Uma consulta ao site da FDA permite localizar o calend�rio de reuni�es do comit� assessor do �rg�o norte-americano. No dia 17 de setembro de 2021, houve apenas uma discuss�o sobre vacinas contra a covid-19, resumida na p�gina oficial da ag�ncia:
“A comiss�o se reunir� em sess�o aberta para discutir o pedido de licen�a biol�gica suplementar da Pfizer-BioNTech para administra��o de uma terceira dose, ou uma dose de refor�o, da vacina contra a covid-19 em indiv�duos com 16 anos ou mais”.
De fato, os pr�prios textos utilizados por Osmar Terra para ilustrar sua alega��o falam sobre uma dose de refor�o, e n�o sobre as duas doses inicialmente previstas, que come�aram a ser administradas a adolescentes nos Estados Unidos em maio de 2021 .
No resumo da reuni�o , dispon�vel no site da FDA, � detalhado que a Pfizer entrou com um pedido para a aplica��o da dose extra no �ltimo dia 25 de agosto, baseando-se em estudos que indicam uma redu��o na prote��o conferida pelas duas doses do imunizante devido � circula��o da variante delta do novo coronav�rus.
Em 17 de setembro, os pesquisadores, epidemiologistas e especialistas que integram o comit� assessor da FDA se reuniram para confrontar o benef�cio dessa dose de refor�o com o “risco potencial” , como resumido no mesmo documento. Em nenhum momento do texto � dito que os especialistas avaliariam a vacina��o de adolescentes de maneira geral.
Na grava��o da reuni�o, transmitida ao vivo no canal da FDA no YouTube, � poss�vel ver que os assessores responderam � pergunta: “Os dados de seguran�a e efic�cia do ensaio cl�nico C4591001 sustentam a aprova��o de uma dose de refor�o da COMIRNARTY administrada pelo menos 6 meses ap�s a conclus�o da s�rie prim�ria para uso em indiv�duos com 16 anos ou mais?” .
A maioria dos integrantes votou “n�o” , avaliando que a necessidade da dose de refor�o ainda n�o foi demonstrada para esse grupo. Por outro lado, se manifestaram a favor de administrar a terceira dose em idosos acima de 65 anos e em outras pessoas com alto risco de desenvolver a forma grave da doen�a.
Nos Estados Unidos, a Pfizer j� possui aprova��o definitiva para administrar a primeira e segunda dose do imunizante a pessoas com 16 anos ou mais e autoriza��o emergencial para vacinar aqueles que t�m entre 12 e 15 anos. No �ltimo dia 20 de setembro, o laborat�rio anunciou que uma dose adaptada do imunizante tamb�m seria “segura” e “tolerada” por crian�as de 5 a 11 anos.
Adolescentes no Brasil
A alega��o come�ou a circular um dia ap�s o Minist�rio da Sa�de brasileiro
voltar atr�s
sobre a orienta��o de vacinar adolescentes contra a covid-19 no pa�s.
No �ltimo dia 2 de setembro, a pasta
havia anunciado
que todos com entre 12 e 17 anos deveriam receber as duas doses do imunizante da Pfizer-BioNTech, ap�s a conclus�o do envio de vacinas para imunizar toda a popula��o adulta brasileira com a primeira dose.
Em 16 de setembro, o minist�rio alterou a orienta��o, recomendando apenas a vacina��o de adolescentes com comorbidades. A mudan�a gerou cr�ticas, com diversas cidades
mantendo a vacina��o
de todos os adolescentes, apesar da recomenda��o contr�ria do Minist�rio da Sa�de.
Nos Estados Unidos, os Centros para o Controle e Preven��o de Doen�as (CDC)
recomendam
que todos com 12 anos ou mais se vacinem contra a covid-19.
“A vacina��o generalizada � uma ferramenta essencial para ajudar a conter a pandemia”,
diz o �rg�o.
Leia mais sobre a COVID-19
- Vacinas contra COVID-19 usadas no Brasil e suas diferen�as
- Minas Gerais tem 10 vacinas em pesquisa nas universidades
- Entenda as regras de prote��o contra as novas cepas
- Como funciona o 'passaporte de vacina��o'?
- Os protocolos para a volta �s aulas em BH
- Pandemia, epidemia e endemia. Entenda a diferen�a
-
Quais os sintomas do coronav�rus?
